Leucémie aiguë myléïde du sujet âgé non éligible à la chimiothérapie intensive

Christophe WILLEKENS
Hématologie Clinique, Institut Gustave Roussy

Stéphane DE BOTTON
Hématologie Clinique, Institut Gustave Roussy

INTRODUCTION[1;4] Les leucémies aiguës myéloïdes (LAM) sont les formes les plus communes des leucémies de l'adulte. Ces LAM constituent un groupe hétérogène d'hémopathies malignes caractérisées par la prolifération clonale et incontrôlée de cellules souches, progéniteurs ou précurseurs hématopoïétiques bloqués dans leur différenciation. Elles ne représentent que 1 % des cancers environ en France. L'incidence des LAM augmente avec les classes d'âges de façon non linéaire. Le taux d'incidence est faible en deçà de 50 ans ( Les LAM du sujet âgé ont été longtemps l'objet d'un désintérêt considérable devant un pronostic extrêmement défavorable à très court terme. Cependant, la mise à disposition de traitements non intensifs efficients dans les classes d'âge de plus de 70 ans représente un intérêt croissant tant dans l'élaboration de protocoles de soin courants que dans l'innovation thérapeutique. Il ne s'agit ici que des LAM non éligibles à des traitements intensifs dont allogreffe. Les traitements d'appoint ne seront pas discutés. DIAGNOSTIC La procédure diagnostique comporte l'examen morphologique conjoint du sang et de la moelle osseuse obtenue par ponction et aspiration sternale ou iliaque (réalisée sous anesthésie locale). Il est impératif d'y associer : - Un immunophénotypage à visée diagnostique (quant au lignage atteint : myéloide, lymphoide B ou T) et de suivi - Un examen cytogénétique +/- FISH à visée diagnostique et de suivi - Un examen de biologie moléculaire (étude de l'ARN et de l'ADN tumoral) à visée diagnostique et de suivi Ces examens sont classants dans les classifications WHO et ICC, pronostiques selon le type de traitement reçus (ELN 2022), orientent le traitement et permettent d'assurer un suivi optimisé (Tableaux 1 et 2). Même chez les sujets âgés ces examens sont essentiels pour la prise en charge. Même chez les sujets âgés ces examens sont essentiels pour la prise en charge.
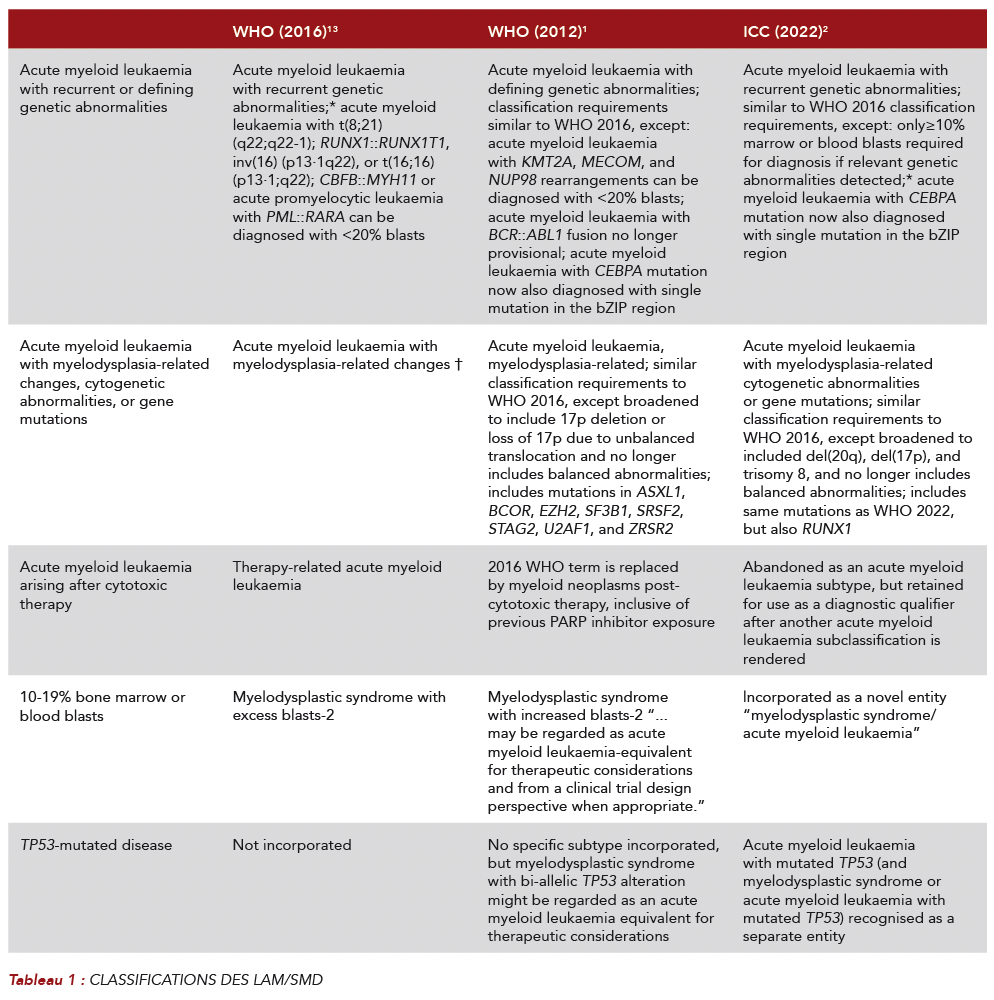

FACTEURS PRONOSTIQUES [5;11] Ils déterminent le plan de traitement a priori.
Facteurs pré thérapeutiques liés au patient L'âge est un pronostic défavorable indépendant. Le score de l'ECOG > 2 et la présence de complications infectieuses au diagnostic (et après initiation du traitement) constituent des facteurs de risque de mortalité précoce. Comorbidités et polymédications sont également des facteurs pronostiques péjoratifs indépendants mais surtout en cas de traitement intensif (incluant la greffe de moelle).
Facteurs pré thérapeutiques liés à la tumeur Chez les sujets âgés, les LAM ont plus de formes de mauvais pronostics lorsqu'un traitement intensif est effectué (par comparaison à des sujets plus jeunes traités de manière équivalente) : - Plus de formes secondaires à d'autres hémopathies myéloïdes (principalement myélodysplasies). - Plus de cytogénétiques défavorables : délétions ou perte des chromosomes 5, 7, ou 17 sont présentes dans 10 à 19 % des cas au sein de caryotypes complexes monosomaux (principalement associés aux formes secondaires). - Moins de cytogénétique favorable ( - Plus de mutations défavorables (ASXL1, BCOR, EZH2, RUNX1, SF3B1, SRSF2, STAG2, U2AF1, ou ZRSR2, principalement associés aux formes secondaires) - Masse tumorale dont le taux de leucocytes est un reflet indirect. En ce qui concerne les patients soumis à un traitement non intensif par agent déméthylant, ces facteurs pronostiques n'ont pas le même impact pronostique.
Réponse au traitement Elle est cruciale et appréciée par l'analyse microscopique du sang et de la moelle, mais également par cytométrie en flux et/ou par biologie moléculaire (pour NPM1 et les transcrits de fusion).
BASES DE LA PRISE EN CHARGE[12-22] Traitements non intensifs en monothérapie Aracytine à faible dose Administrée par voie sous-cutanée 20 mg/12 heures pendant 10 jours, en cycles de quatre semaines. Ce choix n'est pratiquement pas utilisé actuellement car les résultats sont inférieurs à ceux de la 5-azacitidine (5-AZA) (en particulier dans les formes défavorables) et sans bénéfice sur la tolérance.
Agents déméthylants 5-AZA (et DECITABINE non disponible en France) La 5-AZA est un agent déméthylant [inhibition de la méthyltransférase 1 (DNMT1)] et cytotoxique. En monothérapie, dans des formes de LAM avec 30 % de blastes médullaires non prolifératives, les taux de RC + RC avec reconstitution hématopoïétique incomplète (RCi) sont de 27,8 % avec une survie globale médiane de 10,4 mois. Ce traitement est à réserver aux sujets non éligibles aux traitements semi-intensifs.
Traitements semi-intensifs 5-AZA et venetoclax (VEN) Les membres de la famille Bcl-2 sont des régulateurs essentiels de la perméabilisation de la membrane mitochondriale. Les membres anti-apoptotiques-« Bcl2-like survival factors »- comme Bcl-2, Bcl-XL, Mcl-1, préservent l'intégrité de la membrane mitochondriale et sont des modulateurs de la survie cellulaire. Elles sont surexprimées dans les blastes de LAM et contribuent à la résistance aux traitements cytotoxiques. Le VEN est un inhibiteur de BCL2 peu efficace en monothérapie dans les LAM. En revanche son association avec les agents hypométhylants ou l'AraC faible dose a bouleversé la prise en charge des LAM du sujet âgé non éligible aux traitements intensifs. Deux études de phase III en double aveugle VIALE-A et VIALE-C ont permis l'enregistrement de ces combinaisons. La combinaison 5-AZA + Venetoclax augmente significativement le taux de réponse (66,4 % versus 28,3 %), et la survie globale médiane (14,7 mois versus 9,6 mois) par rapport à la 5-AZA + Placebo. Il s'agit d'un traitement ambulatoire mais, attention, semi intensif. Le profil de toxicité est en effet moins favorable que celui de la 5-AZA seule. Les durées de cytopénies sont ainsi significativement plus longues avec plus de neutropénies fébriles de grade ≥ 3. L'utilisation quotidienne de ce traitement vise néanmoins à conserver l'efficacité de l'association mais en diminuant sa toxicité en modulant la durée du VEN ou l'espacement entre les cures. Des essais tentent aussi d'explorer la possibilité de moduler la bithérapie en fonction de la maladie résiduelle ou d'envisager des durées fixes de traitement car, à ce jour, cette stratégie est recommandée jusqu'à progression. La combinaison AraC faible dose et venetoclax donne des résultats significatifs mais moins impressionnants que la combinaison 5-AZA + VEN et est, de ce fait, beaucoup moins usitée. Les facteurs pronostiques associés à la survie diffèrent de ceux liés aux traitements intensifs et incluent les mutations de TP53 et des mutations de signalisation (FLT3-ITD ; NRAS ; KRAS). On distingue ainsi 3 groupes dont la survie globale diffère significativement (Figure 1) : - Si les mutations TP53 sont présentes : ce groupe ne bénéficie que peu ou pas de la combinaison 5-AZA + Venetoclax où la survie globale médiane est de 5.5 mois. - Mutations FLT3-ITD ; NRAS ; KRAS (mais SANS mutation TP53) : le bénéfice est modéré avec survie globale médiane de 12 mois. - En l'absence de mutations FLT3-ITD ; NRAS ; KRAS ou TP53 : le bénéfice de la combinaison AZA + VEN est considérable avec une survie globale médiane de 26 mois.
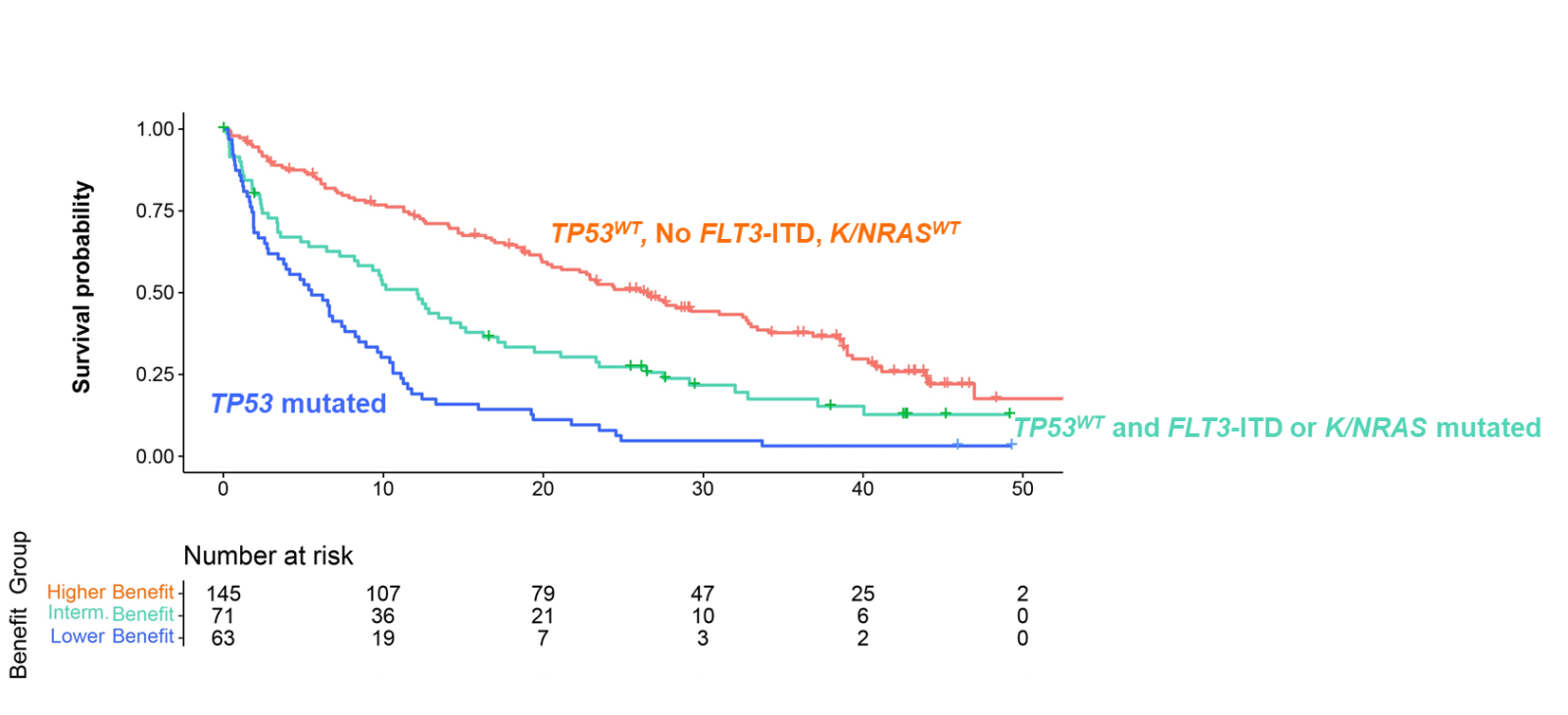
Figure 1 : Stratification du risque selon le statut mutationnel patients recevant 5-AZA + Venetoclax - Döhner H, ASH 2022 https://doi.org/10.1182/blood-2022-169509
Thérapies ciblées [20-21] L'accès à la génomique permet de mieux prédire la réponse et la durée de réponse au traitement. De plus elle permet l'accès aux traitements ciblés approuvés en première ligne ou en rechute.
Inhibiteur d'IDH1 Le seul traitement ciblé sur une mutation, en première ligne de traitement, dans cette population est l'inhibiteur d'IDH1, l'ivosidenib (IVO) en combinaison avec la 5-AZA. Cela représente environ 10 % des cas de LAM du sujet âgé. L'étude de phase 3 randomisée AGILE, associait IVO 500 mg/jour en continu + 5-AZA pendant 7 jours versus 5-AZA + placebo. La survie globale médiane était de 24,0 mois dans le bras IVO versus 7,9 mois dans le bras placebo. Le profil de tolérance de la combinaison IVO + 5-AZA est meilleur que la 5-AZA seule quant aux épisodes infectieux et cela est dû à un taux de réponses significativement meilleur avec une récupération de neutrophiles fonctionnels plus rapide. Il est donc impératif d'attendre (hors urgence) les résultats de la recherche de mutation IDH1 avant d'initier un traitement de la LAM.
Les inhibiteurs de FLT3 Les mutations de type FLT3-ITD confèrent une résistance à la chimiothérapie conventionnelle, surtout en cas de rechute. Le Gilteritinib, inhibiteur anti-FLT3, est approuvé dans les LAM FLT3 mutées en situation de rechute ou de situation réfractaire et les mutations de FLT3 doivent être recherchées de nouveau en cas de récidive, y compris chez les sujets de plus de 65 ans qui peuvent bénéficier de ce traitement.
CONCLUSIONS La prise en charge des LAM du sujet âgé requiert désormais des mesures diagnostiques identiques à celles du sujet jeune (biologie moléculaire). L'analyse génétique des LAM permet en effet d'adapter au mieux la thérapeutique et de faire bénéficier aux patients des avancées thérapeutiques réalisées ces dernières années (Figure 2).
